



1、使用面積較小的蓋玻片制作標(biāo)本時,應(yīng)使用ProLong Diamond Antifade Mountant 等凝固型封片劑封片。使用凝固型封片劑可以避免標(biāo)本移動。
2、應(yīng)盡量使用平場復(fù)消色差(Plan-APO)物鏡來采集圖像。使用平場復(fù)消色差(Plan-APO)物鏡可以獲得較平整的和色差較小的圖像。
3、在采集熒光圖像時盡量不要同時采集 DIC 圖像以免降低圖像分辨率和影響圖像亮度。
4、在進行熒光亮度定量分析實驗時,所有的采圖參數(shù)(光路設(shè)置、激光強度、PMT 增益、PMT Offset、平均次數(shù)、Zoom 、Pinhole 等)都必須保持一致,建議使用陽性標(biāo)本(熒光亮度最亮的標(biāo)本)來設(shè)置參數(shù),避免熒光亮度過飽和。應(yīng)盡量預(yù)訂足夠長時間的實驗時間,在一次實驗中完成所有熒光定量分析標(biāo)本的成像。
5、在共聚焦采圖時,如無特殊原因 Pinhole 應(yīng)該設(shè)置在 1 Airy Unit 位置,PMT Offset 應(yīng)該設(shè)置在 0 位置,PMT Gain 分別設(shè)置在 50-150 (for NIKON Ti-A1R、NIKON FN1- A1R)、600-800 (for Olympus FV-1000)、40-60%(for Olympus FV-10i)、600-700 (for Zeiss LSM 510)。
6、在共聚焦活標(biāo)本采圖時,可以根據(jù)實驗需要適當(dāng)增大 Pinhole 、降低激光強度、增加 PMT Gain、降低采圖分辨率、增加采圖速度以減小激光對細(xì)胞活性的影響。
7、在使用 Prairie Two-photon 顯微鏡雙光子采圖時,PMT Gain 應(yīng)該設(shè)置在 600-800,PMT Offset 設(shè)置在 1.17 左右,并使用 HiLo Lookup Table 檢查圖像亮度,避免背景過低或圖像過飽和。
8、在活細(xì)胞成像時應(yīng)盡量使用水鏡,避免球差引起的分辨率變差、結(jié)構(gòu)變形(拉長或縮短)。
9、在多標(biāo)記標(biāo)本熒光成像時,要使用序列掃描來減少串色。串色只能盡量減少不可能完全避免,所以還必須使用單熒光標(biāo)記標(biāo)本作為對照來檢查是否串色, 并用軟件來進行串色校正。
10、不要用 Live-scan 長時間掃描標(biāo)本、也不要長時間在熒光燈下觀察標(biāo)本,以防標(biāo)本漂白。
11、設(shè)置參數(shù)要 1 個通道 1 個通道設(shè)置,NIKON 共聚焦顯微鏡應(yīng)使用 Preview 和 Capture 分別設(shè)置預(yù)覽參數(shù)和正式采圖參數(shù)。采集預(yù)覽圖像時應(yīng)使用低分辨率掃描,不要使用高分辨率掃描或平均。
12、在多熒光標(biāo)記標(biāo)本成像時(尤其是使用 Plan-APO 60x 高數(shù)值孔徑物鏡高分辨成像時),必須使用多色熒光小球標(biāo)本為對照來檢查色差引起的圖像在 XYZ 方向上的偏移。色差只能盡量避免(如:使用 Plan-APO 物鏡、使用波長比較接近的488 nm 和561 nm 激光來采圖等)不可能完全避免。色差一般為 幾十-幾百 納米(視不同的顯微鏡構(gòu)架、物鏡類型、激發(fā)光波長的不同而不同),高分辨率成像實驗的圖像必須使用軟件來進行色差校正。
13、高分辨率圖像采集和活細(xì)胞圖像采集的圖像(包括Z-stack、Time-series、Two-photon image), 可以使用反卷積軟件來進一步提高分辨率或降低噪聲(提高信噪比)。反卷積的效果與原始圖像的采圖分辨率密切相關(guān),一般采圖分辨率需要達到物鏡極限分辨率的 1/3-1/4。
圖像的分辨率和信噪比對熒光共定位分析至關(guān)重要。熒光共定位分析實驗必須使用高數(shù)值孔徑物鏡成像。圖像必須經(jīng)過反卷積、色差校正、串色校正等處理。需要做反卷積處理的同學(xué)請找胡謙老師討論實驗和確定采圖參數(shù)。
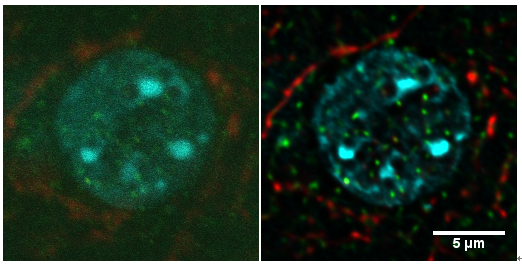
左圖為原始圖像(此標(biāo)本熒光標(biāo)記比較弱,無法獲得高信噪比的圖像), 右圖為經(jīng)過反卷積和色差校正后的圖像,使用 OLYMPUS FV-1000 PLAPON 60xOil NA. 1.42 物鏡, 采圖分辨率 xy=0.069 um/pixel, z=0.25 um/pixel
14、 所有光學(xué)成像實驗都必須設(shè)計和完成正對照實驗和負(fù)對照實驗來保證光學(xué)成像實驗結(jié)果的正確性和準(zhǔn)確性。http://en.wikipedia.org/wiki/Scientific_control
Positive controls are groups where a phenomenon is expected. That is, they ensure that there is an effect when there should be an effect, by using an experimental treatment that is already known to produce that effect (and then comparing this to the treatment that is being investigated in the experiment).
Negative controls are groups where no phenomenon is expected. They ensure that there is no effect when there should be no effect. To continue with the example of drug testing, a negative control is a group that has not been administered the drug of interest. This group receives either no preparation at all or a sham preparation (that is, a placebo), either an excipient-only (also called vehicle-only) preparation or the proverbial "sugar pill." We would say that the control group should show a negative or null effect.
-----------------------------------------------------------------
附:Fura-2 AM Loading Protocol
分 子 式: C44H47N3O24
分 子 量: 1001.85
外 觀: 黃色或橙黃色粉末
Loading cells with Fura-2
------------------------------------------------------------------
General Information on Fura-2 AM ester:
Fura-2 is a high-affinity (Kd = 220 nM) Ca2+ dye.
AM ester = acetoxymethyl ester; The AM ester makes the dye membrane permeable because it caps hydrophilic carboxyl groups to form esters. Once the dye is taken up into cells, the esters are cleaved by intracellular esterases and the dye is trapped inside.
Excitation ratiometric imaging of Fura-2 is carried out by using 340/26 nm and 380/10 nm excitation filters, a 455 nm dichroic mirror (must have good reflectivity down to approximately 330 nm), and a 535/40 nm emission filter.
Fura-2 is light sensitive so store in lightproof manner (e.g., wrapped in tin-foil) at – 20 oC.
Both Fura-2 and Pluronic F-127 can