發布時間:2020-02-12
作者 | 中國科學院腦科學與智能技術卓越創新中心 唐騁
最近受新冠病毒的影響,很多朋友可能都宅在家里,這時候你可能會很生氣,自然界怎么會有病毒這種討厭的東西,這玩意兒到底是怎么演化出來的呀?
誒,這個問題可能會讓你重新思考生命的含義。
了解演化的朋友應該都知道,只要往上追溯,任何兩個生物都能追溯到某個共同祖先,而祖先還能繼續溯源到祖先的共同祖先,最終構建起一棵足以囊括古今眾生的演化之樹。
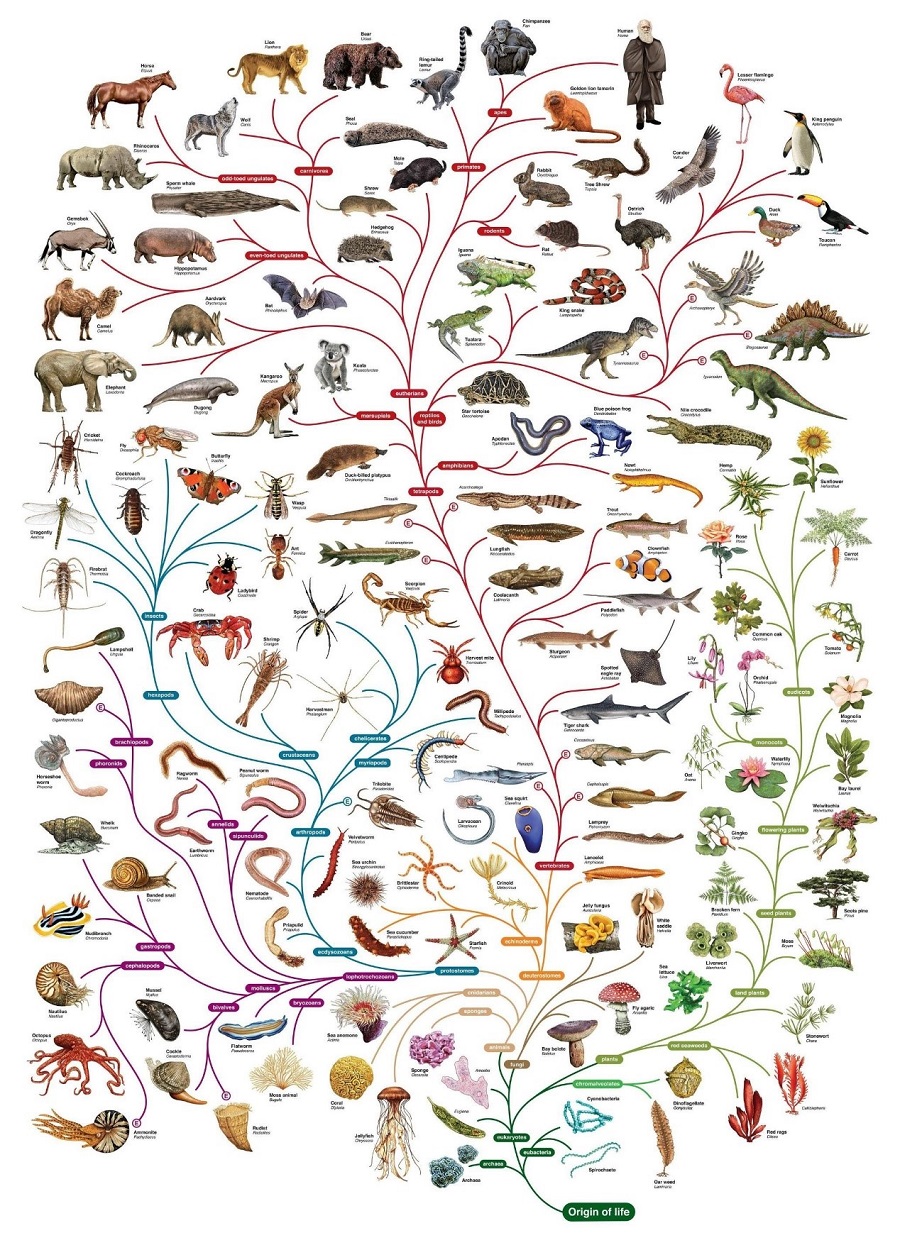
大家熟悉的演化樹大概就是這個樣子的(圖片來源:Pinterest;上傳者:Michelle West)
然而病毒卻似乎不在這棵樹上。大部分病毒的結構很簡單,比如說這次的新型冠狀病毒,它的結構就是一個蛋白質外殼包著一些遺傳物質,外面再加一層包膜。它們會通過呼吸感染呼吸道粘膜上皮細胞,利用自己的包膜混進細胞內部,然后劫持細胞來制造構建自身所需的各種零件,最后將這些零件組裝成恒河沙數的自身,脫離細胞,臨了還要順一塊細胞膜披在自己身上以便下一次作案。這種奇怪的生活方式讓我們難以將其置于演化之樹的任何地方。
病毒是生物嗎?它們又從何而來呢?
下面,我們就來看看病毒起源的三個假說。
假說一:遠古分子生命的復仇之魂
病毒的故事或許還要從遠古說起。在那個了無生機的地球上,海洋占據了世界的絕大部分,而無垠的大海之下是數億年連綿不斷的火山活動。在某些機緣巧合之下,海水中產生了史上第一批有機大分子,從而點燃了生命的星星之火。

“hydrothermal vent”的圖片搜索結果
生命最初或許就誕生在類似這樣的地方,Credit: Ocean Exploration Trust
慢慢的,有一些大分子,比如說RNA,DNA以及蛋白質開始或獨立或彼此協作地復制自身,這個階段可以稱為“分子生命”。然而在一片祥和的分子生命中卻產生了一個異類,那就是包括現存所有生物的最近共同祖先“露卡”(LUCA)在內的一些分子生命,它們發展出了一個改變了生命法則的結構,那就是細胞。擁有膜結構的細胞可以更好地保護其中嬌弱的RNA和蛋白質等核心大分子,極大增強了這些生物的適應力,意味著它們會把原始的分子生命摁在地上摩擦。
而有一種假說(The Virus-First Hypothesis)就認為,病毒正是原始分子生命世界的遺民,它們在在最后一刻創造出了寄生的生活方式,反過來利用了敵人的細胞結構,宛如一群遠古的復仇之魂,對于奪取它家園的族裔作著永恒的抗爭。
這個假說一度十分盛行,畢竟病毒的構造是如此簡單,乃至簡陋,它們與細胞生命的差異又是如此巨大。像引起這次疫情的冠狀病毒以及每年冬天都會來報到的流感病毒,它們的遺傳物質甚至是RNA,而不像細胞生物那樣利用DNA來承載自己的遺傳信息。
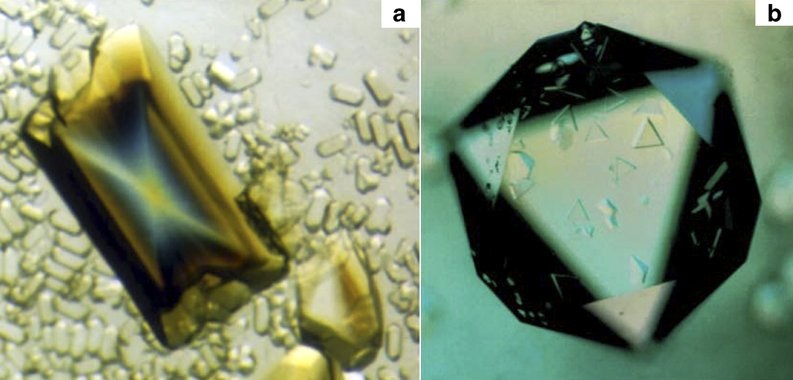
有些病毒經提純后還能形成結晶,這對于細胞生物是無法想象的(圖片來源:Alexander McPherson & Lawrence James DeLucas)
更實錘的證據來自于“擬病毒”(Virusoid),它就是一個RNA分子。擬病毒沒辦法直接感染細胞,但是它可以感染病毒,確切地說是在某些病毒感染細胞的時候通過搭便車來順便復制自己、擴散自己,從而能引發一些諸如人類丁型肝炎之類的疾病。
然而這個熱血的病毒起源故事卻隨著分子生物研究學的深入而顯得不再那么完美……
假說二:“叛逃”的基因
基因這濃眉大眼的也能叛變?對,在這個假說(The Progressive Hypothesis)里,基因為了讓自己流傳下去什么事情都做得出來。
細菌中廣泛存在一種名叫“質粒”(plasmid)的小片段環狀DNA,這些基因基本上就是一群打工仔臨時工,細菌隨時可以從環境中吸收它們為己所用,也隨時可以趕走它們。

在很多細菌中,除了自身原本的DNA(紅色部分)以外,還經常會有一些小片段的環狀DNA(橙色),那些被稱為質粒(圖片來源:作者繪制)
于是在漫長的演化中,有些質粒學會了一件事:我們不要一輩子打工!這些質粒從打工仔變成了二五仔,反過來把它們的細菌老板給劫持了,奪走了細菌所有的營養來復制自身。隨著時間推移,有些質粒就變成了病毒。

細菌經常會遭受一類叫做“噬菌體”(Phage)的病毒感染,有些觀點認為噬菌體來源于質粒(圖片來源:Quanta Magazine)
而我們人類以及所有動物、植物的細胞和細菌很不一樣,我們都屬于“真核生物”,細胞當中并沒有細菌那樣的質粒,但還是有那么一些基因蠢蠢欲動。它們不肯在染色體上好好待著,而是在細胞核里左右橫跳,一會兒跑到這個染色體上,一會兒跑到那個染色體上。不過這幫調皮搗蛋的基因倒是有一個仙風道骨的名字——轉座子(transposon)。
根據分子生物學檢測,很多轉座子都擁有和病毒非常相似的基因序列,兩者將自己整合進宿主細胞染色體的機制也高度相似。尤其是其中的“病毒樣逆轉錄轉座子”(Retrotransposon)與某些病毒簡直相似到了令人發指的程度,唯一的不同只是這些轉座子還不能像病毒一樣在細胞之間遷移而已。
然而病毒的身世到這里卻依舊撲朔迷離,因為它們根本就不遵循一般生物的演化模式。
病毒感染的一般流程是:把自己的基因注入宿主細胞當中,然后利用宿主細胞復制自己的基因,并且制造構建病毒顆粒所需的各種材料,最后操控細胞將病毒顆粒的各個零件連同病毒的基因一起包裝成新的病毒顆粒,釋放出去感染別的細胞。
但是在這個過程中,病毒每時每刻都在和各種生物交換基因。
比如說病毒在指揮宿主細胞包裝病毒顆粒的時候,有時候會把一些宿主細胞的DNA給一塊包進去,或者不小心在宿主細胞當中留一點點自己的基因。哺乳動物中有一個用來阻止母體免疫系統攻擊胎兒的基因,就是某個病毒在一億多年不小心落在我們細胞中的。而在病毒跨物種傳播的時候,經常導致基因從一個物種轉移到另一個物種,所以,“轉基因”這件事都是自然界玩剩下的。
然而也正是因為病毒的轉基因如此之頻繁,讓人不得不重新思考,病毒真的是叛逃的基因嗎?我們會不會從一開始就搞錯了邏輯關系。那些轉座子啥的,也許并不是不安其室的自身基因,反而是偶然留在細胞中的病毒基因呢?
假說三:病毒也許是沉淪的細胞生物
進入21世紀以后,一系列發現開始讓科學家愈發意識到病毒的起源還有別的可能性。
2003年,科學家發現了一種非常不講道理的病毒——“擬菌病毒”(Mimivirus),這個病毒的體型達到了0.4到0.5微米,在顯微鏡下看都快跟細菌差不多了。引發這次疫情的冠狀病毒都被認為是比較大的一類病毒了,體型也不到0.1微米。

龐大的擬菌病毒(圖片來源:Haitham Sobhy et al. 2015)
2008年,科學家發現了第二種大病毒,將其命名為 “媽媽病毒”(Mamavirus),從此一種又一種“大病毒”(Giant Virus)開始接二連三地出現在人類的視野中,到2013年發現的“潘多拉病毒”(Pandoravirus)更是把最大病毒的記錄刷到了1微米以上。
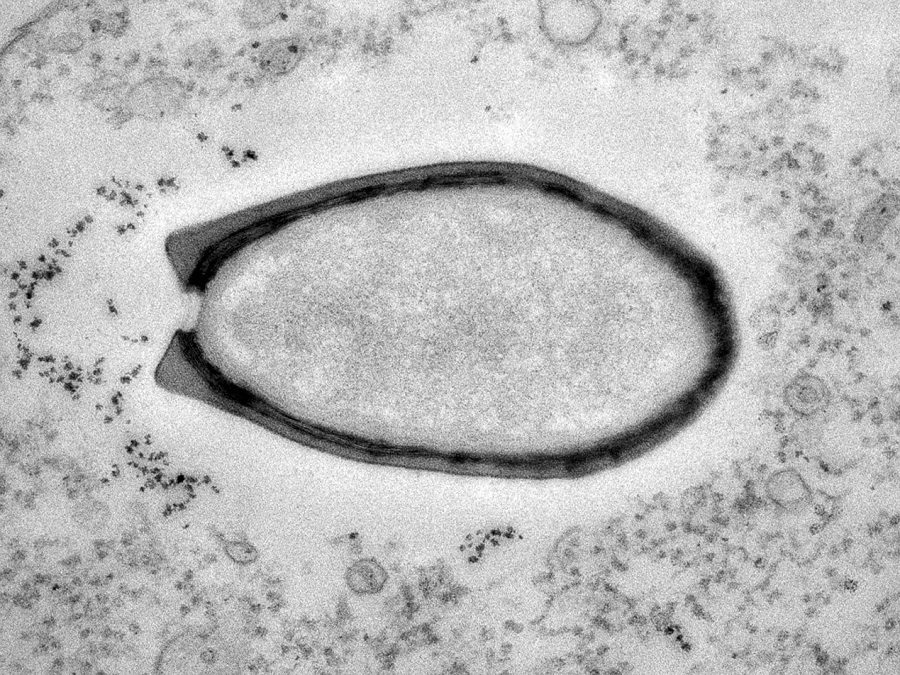
目前已知最大的病毒“潘多拉病毒”,它看上去和一個細菌幾乎沒什么區別(圖片來源:美國國家地理;作者:Chantal Abergel和Jean-Michel Claverie)
從此,病毒與某些單細胞生物的界限開始變得模糊了起來,比如說“擬菌病毒”的結構與基因和一類叫做“古菌”的單細胞生物非常相似,唯一的不同是,擬菌病毒丟失了一部分自主完成細胞分裂的關鍵基因,所以不得不寄生在其它生物的細胞當中,利用宿主的細胞來生長繁殖。
于是就有了病毒起源的第三種假說(The Regressive Hypothesis),認為病毒本質上是墮落的生物。有些單細胞生物在長期寄生生活中,逐漸退化掉絕大部分細胞結構,最終變成了這種活死人一般的樣子,而像擬菌病毒之流就是剛剛開始墮落的古菌。
在我們的演化中,病毒留下了深深的烙印
那么,病毒究竟應該是遠古的復仇之魂,還是叛逃的基因,亦或是墮落的生物呢?這三種假說都有合理之處,同時也存在著不能解釋的問題。也許,病毒的起源故事遠比這一切假說都更加復雜,甚至未必有著唯一的來源。
而這也給科學家的研究帶來了數不清的麻煩,因為我們很難將病毒像細胞生物那樣根據親緣關系來分類,所以大部分病毒還是以它們的形態和引發癥狀來粗糙歸類,比如說冠狀病毒就是因為在電子顯微鏡下看起來有很多凸起像皇冠一樣而得名。
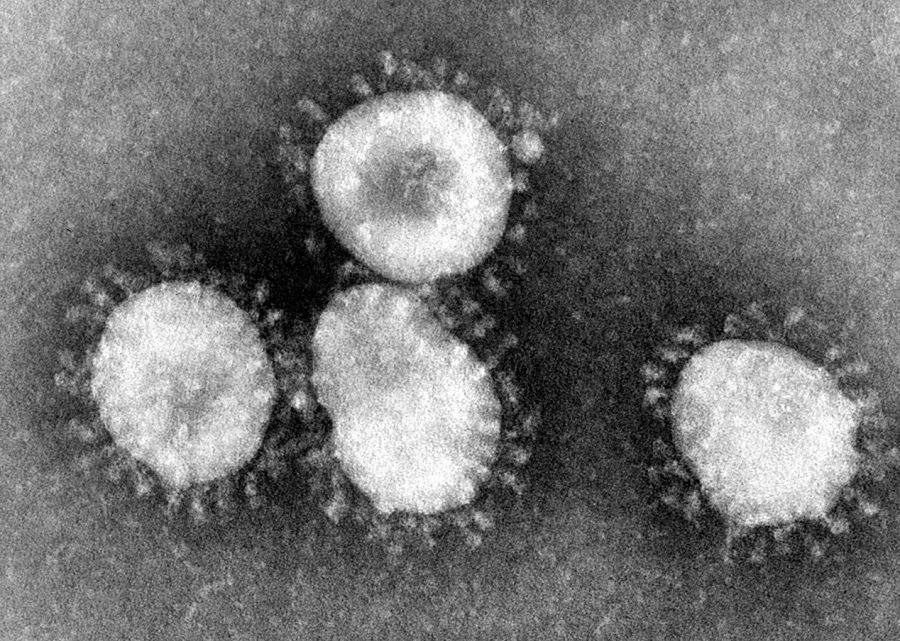
新型冠狀病毒在電子顯微鏡下就是這樣的,看上去有很多凸起。圖源:CDC/Dr.Fred Murphy
我們可能永遠也弄不清病毒從何而來,但是病毒卻真真切切地在我們的演化中留下了深深的烙印。
由于病毒無比強大的變異能力,我們永遠也無法預測何時何地會出現一個對我們有致命威脅的病毒,最終逼得很多生物不得不采取一些用變異打敗變異的手段。
比如說有性生殖。有性生殖帶來最直接的后果就是可以讓我們的每一個后代的基因都能打亂重排,盡可能保障所有后代不至于被一種病毒一鍋端了。病毒與生物的軍備競賽也一直是演化的最強推手,病毒還打破了生殖隔離的壁障,讓基因得以在不同的生物中流動。
所以,病毒雖不屬于演化之樹上的任何一個枝丫,但它們宛若是圍繞在演化之樹上的流螢與鬼魅,在這棵樹上處處都留下了自己的痕跡。
那么為什么致命病毒總是來自于野生動物呢?讓我們從演化的角度分析一下。
“最好”的病毒,是既不引起太嚴重的癥狀(不然搞死了宿主自己也完蛋),但也不能太溫和(畢竟宿主身上往往同時寄生著別的病毒,搶資源的時候該下的狠手還是得下)。所以在漫長的演化中,這種博弈會促使病毒最終與宿主達成某種默契,比如說人類與可能會引起普通感冒的鼻病毒就屬于這種關系。
但是,病毒會變異,有些變異會導致病毒的宿主改變。病毒與新的宿主沒有長期磨合的默契,就會出現“下手沒輕沒重”的問題,其中有些下手特別重的就會給宿主帶來致命疾病。
在長期的演化中,人類已經和那些從遠古祖先開始一路陪伴的病毒達成完美默契了,與從家畜那里來的病毒,比如麻疹、流感等等,磨合得還不完美,但多少有點默契,所以極少引起很嚴重的疫情。唯獨來自于野生動物的病毒跟我們絲毫沒有一丁點磨合,因此引起大瘟疫的疾病幾乎全部來自野生動物。
因此希望大家平時盡量遠離野生動物,包括流浪動物,更不要去飼養、食用野生動物,不然這些野生動物身上的病毒可就保不準拿你來試刀子啦。
愿小伙伴們都能用知識武裝起自己,加油!
參考資料:
1.Wessner, D. R. (2010). The origins of viruses. Nature Education, 3(9), 37.
2.Suchard, M. A., Lemey, P., Baele, G., Ayres, D. L., Drummond, A. J., & Rambaut, A. (2018). Bayesian phylogenetic and phylodynamic data integration using BEAST 1.10. Virus evolution, 4(1), vey016.
3.Duffy, S. (2018). Why are RNA virus mutation rates so damn high?. PLoS biology, 16(8), e3000003.
4.Stern, A., Te Yeh, M., Zinger, T., Smith, M., Wright, C., Ling, G., ... & Andino, R. (2017). The evolutionary pathway to virulence of an RNA virus. Cell, 169(1), 35-46.
5.Villarreal, L. P., & DeFilippis, V. R. (2000). A hypothesis for DNA viruses as the origin of eukaryotic replication proteins. Journal of Virology, 74(15), 7079-7084.
6.Koonin, E. V., & Martin, W. (2005). On the origin of genomes and cells within inorganic compartments. TRENDS in Genetics, 21(12), 647-654.
7.Kolakofsky, D. (2015). A short biased history of RNA viruses. RNA, 21(4), 667-669.
8.Van Etten, J. L., Lane, L. C., & Dunigan, D. D. (2010). DNA viruses: the really big ones (giruses). Annual review of microbiology, 64, 83-99.
9.Prangishvili, D., Forterre, P., & Garrett, R. A. (2006). Viruses of the Archaea: a unifying view. Nature Reviews Microbiology, 4(11), 837-848.
10.Canchaya, C., Fournous, G., Chibani-Chennoufi, S., Dillmann, M. L., & Brüssow, H. (2003). Phage as agents of lateral gene transfer. Current opinion in microbiology, 6(4), 417-424.
11.Gerstein, M., & Zheng, D. (2006). The real life of pseudogenes. Scientific American, 295(2), 48-55.
12.Chuong, E. B., Elde, N. C., & Feschotte, C. (2017). Regulatory activities of transposable elements: from conflicts to benefits. Nature Reviews Genetics, 18(2), 71.
13.Sanmiguel, P., & Bennetzen, J. L. (1998). Evidence that a recent increase in maize genome size was caused by the massive amplification of intergene retrotransposons. Annals of Botany, 82, 37-44.
14.Bell, P. J. L. (2001). Viral eukaryogenesis: was the ancestor of the nucleus a complex DNA virus?. Journal of Molecular Evolution, 53(3), 251-256.
15.黃耀偉, 李龍, & 于漣. (2004). 人類及動物 RNA 病毒的反向遺傳系統 (Doctoral dissertation).
16.Villarreal, L. P., & Villareal, L. P. (1997). On viruses, sex, and motherhood. Journal of Virology, 71(2), 859.
17.Dupressoir, A., Lavialle, C., & Heidmann, T. (2012). From ancestral infectious retroviruses to bona fide cellular genes: role of the captured syncytins in placentation. Placenta, 33(9), 663-671.
18.La Scola, B., Audic, S., Robert, C., Jungang, L., de Lamballerie, X., Drancourt, M., ... & Raoult, D. (2003). A giant virus in amoebae. Science, 299(5615), 2033-2033.
19.Xiao, C., Chipman, P. R., Battisti, A. J., Bowman, V. D., Renesto, P., Raoult, D., & Rossmann, M. G. (2005). Cryo-electron microscopy of the giant Mimivirus. Journal of molecular biology, 353(3), 493-496.
20.Schulz, F., Roux, S., Paez-Espino, D., Jungbluth, S., Walsh, D., Denef, V. J., ... & Woyke, T. (2020). Giant virus diversity and host interactions through global metagenomics. Nature, 1-7.
21.Brahim Belhaouari, D., Baudoin, J. P., Gnankou, F., Di Pinto, F., Colson, P., Aherfi, S., & La Scola, B. (2019). Evidence of a Cellulosic Layer in Pandoravirus massiliensis Tegument and the Mystery of the Genetic Support of Its Biosynthesis. Frontiers in Microbiology, 10, 2932.
22.Forterre, P. (2010). Giant viruses: conflicts in revisiting the virus concept. Intervirology, 53(5), 362-378.
23.Shabbir, M. Z., Rahman, A. U., & Munir, M. (2020). A comprehensive global perspective on phylogenomics and evolutionary dynamics of Small ruminant morbillivirus. Scientific Reports, 10(1), 1-17.
 附件下載:
附件下載: