發布時間:2022-05-20
從小嬰兒咿呀學語、蹣跚學步到嬉笑怒罵、經歷生活敲打的酸甜苦辣,無一不需要大腦的參與。大腦作為情緒、思想、行動等的載體,是宇宙中最迷人也最復雜的研究對象。如果說“想象”存在停靠的位置,那么大腦毫無疑問便是起源。然而,記憶是如何形成并存儲的,意識是什么,情緒是如何產生的——這些日常生活中我們習以為常的事件的發生背后都隱含著神經科學領域的重要科學問題。
從17世紀胡克通過顯微鏡第一次觀察到植物細胞到19世紀施萊登、施旺建立起細胞學說,人們逐漸認識到:細胞是生物體結構和功能的基本單位。然而,由于缺乏使神經系統“顯形”的有效染色方法,人們對神經系統的基本組成知之甚少。當時科學界普遍認可約瑟夫·格拉赫(Joseph von Gerlach)基于他的氯化金染色法提出的網狀學說,即像人體的血管網絡一樣,神經組織是由神經細胞融合而成的連續網絡。1873年,卡米洛·高爾基(Camillo Golgi)發明重鉻酸銀染色法(后稱高爾基染色法),可以使少量神經元(1-5%)染色,從而使完整的神經元形態暴露于世人眼中——然而高爾基對此并不懷疑網狀學說的正確性。1887年,圣地亞哥·拉蒙·卡哈爾(Santiago Ramón y Cajal)第一次接觸到高爾基染色的神經組織樣本,并大受震撼——此后他基于改良的高爾基染色方法對大量腦組織切片進行細致的觀察,向網狀學說發起挑戰,指出神經細胞是相互獨立的單位。
在卡哈爾一系列發現的基礎上,1891年,瓦爾岱耶(Wilhelm von Waldyer)正式提出“神經元”的概念,并建立起神經元理論。1906年,為表彰高爾基和卡哈爾在神經系統結構的解析中做出的杰出貢獻,他們二人共同獲得諾貝爾生理學或醫學獎。即使是在頒獎禮上,二人仍針鋒相對,為自己的學說進行辯論。而直到電子顯微鏡發明,這一學術爭論才真正一錘定音——神經元學說成為現代神經科學發展的基本理論。卡哈爾由此被認為是現代神經科學之父。

卡米洛·高爾基與圣地亞哥·拉蒙·卡哈爾(左)和卡哈爾繪制的神經元(右)
如今我們已經知道,正是大腦中小小的神經元通過突起相互聯系組成了復雜的神經網絡,處理來自體內外的紛繁復雜的信息,嚴密監控、指導著機體的正常運轉。據估計,哺乳動物的大腦有數以百萬計的細胞,人腦擁有860億個神經元。DNA 雙螺旋結構發現人之一、諾貝爾生理學或醫學獎獲得者Crick和Jones在給 Nature 的評論中寫道:“我無法忍受我們沒有繪制出人類大腦的連接圖。沒有它,很難有希望能了解我們的大腦是如何工作的。”——我們要想理解大腦的工作原理,繞不開對于大腦結構的精細解析。而神經元作為研究大腦功能的基本單位,對于其結構的認識無疑有助于理解大腦的信息組織架構——正像是唯有明白了電視機內部每個元件如何連接組織,我們才能掌握電視機如何播放圖像、聲音,如何接受外界的指令。小鼠作為生命科學領域的明星模式動物,解析它的全腦神經元結構特征自然便成為了科學家們首先關注的科學問題。因此,正如同卡哈爾一樣,我們面臨的問題是選擇一項合適的技術實現對神經元的可視化。
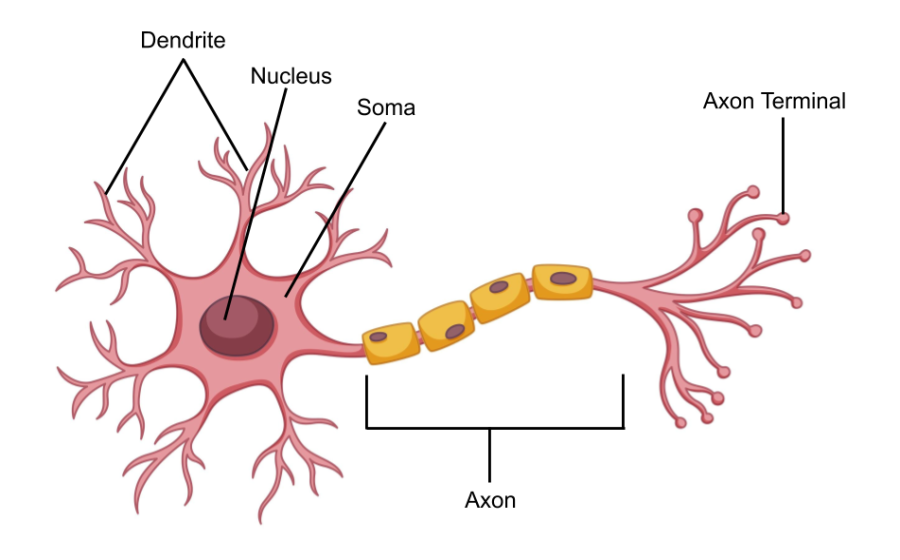
神經元結構圖
一個典型的神經元由胞體、樹突、軸突構成。其中,樹突粗而密集,位于胞體附近,接收其他神經元的信息輸入。軸突則又長又細,可以延伸很遠,軸突的末端可以形成突觸前末梢,與另一個神經元的樹突或者胞體形成突觸連接,通過釋放突觸遞質參與神經元之間的信息傳遞。神經元胞體通常為十幾到幾十微米不等,軸突長度卻可以達到厘米級別,而其直徑卻僅為0.2-0.5微米。也就是說,為了能看清神經元的軸突走向,我們至少應該選擇達到微米級的成像手段。目前,電鏡作為成像分辨率最高的技術手段,可以實現納米級別的成像,也已經應用到小動物如線蟲、果蠅的神經元連接圖譜的研究中——但是僅僅小鼠的腦體積就相當于線蟲腦體積的一千萬倍,更不用說腦容量更大的靈長類了。考慮到小鼠全腦范圍成像所需成本、時間及產生的龐大的數據量——電鏡成像很明顯不適用。為了滿足在全腦尺度上解析神經元連接圖譜,科學家們將視線投向光學成像。
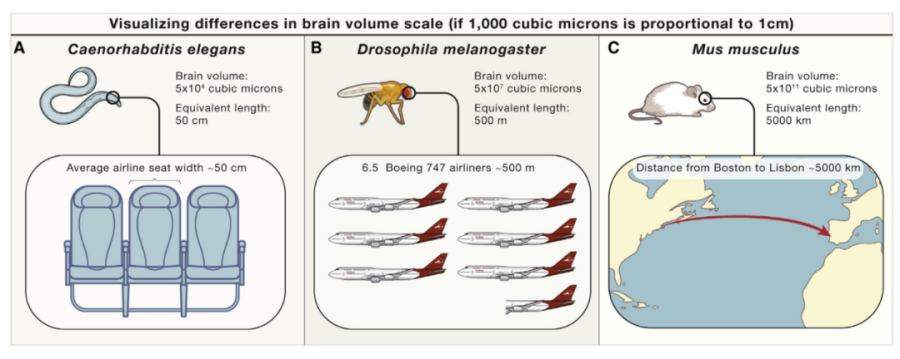
線蟲、果蠅、小鼠腦容量比較
2010年,華中科技大學駱清銘教授團隊利用自主研發的顯微光學切片斷層成像(micro-optical sectioning tomography, MOST)技術成功實現小鼠全腦的高分辨率圖譜繪制。他們利用改良的高爾基染色方法對鼠腦進行染色,并利用Spurr樹脂對鼠腦進行包被。為了繞過光學成像的成像深度限制,他們創造性地提出了“邊切片邊成像”的策略。在成像時,金剛石刀片將固定好的小鼠腦子切成厚度為1微米、寬450微米的條狀組織薄片,隨后由光學顯微鏡對切好的薄片進行成像。歷經242小時,完成對小鼠全腦的成像,通過后期的數據處理,可以將切片圖像拼接最終重構形成三維立體的小鼠全腦圖譜。
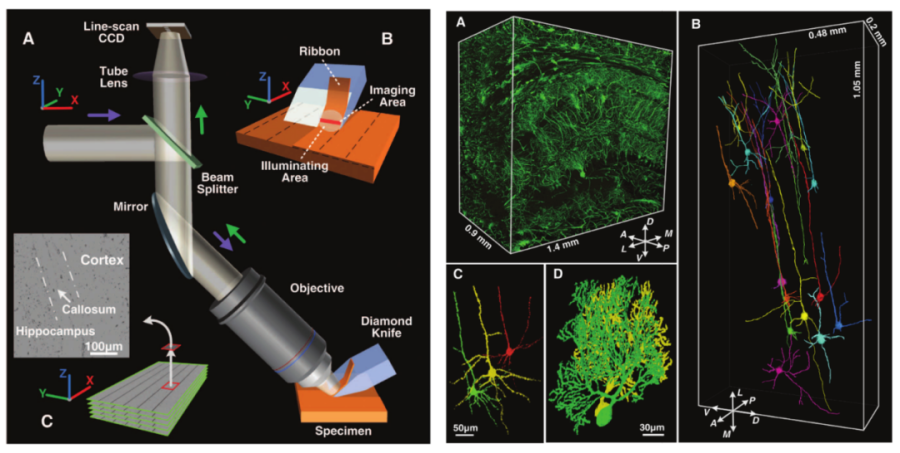
MOST技術成像原理示意圖(左)及小鼠腦成像結果圖展示(右)
雖然MOST技術實現了小鼠全腦的神經元成像,但是在實際研究中科學家們更傾向于利用熒光蛋白標記某些神經元而不是利用染色的方法對全腦神經元進行染色。因此發展可以實現熒光成像的MOST技術即fMOST(fluorescence micro-optical sectioning tomography)則成為他們下一階段的目標。
與染色劑所需的明場成像不同,熒光蛋白由于對溫度、pH更加敏感,稍有不慎就可能導致信號淬滅,對于成像的要求也就更高了。為此,他們改進了鼠腦在成像前的處理和包被方法,最大限度地減少熒光信號的丟失,同時保證組織薄片具備合適的硬度,避免組織過薄發生變形影響成像效果。為了能準確獲得神經元胞體及突起的在大腦中的定位信息,他們也利用大腦中的標志性位置結合MRI和小鼠標準腦圖譜進行了相應的計算和轉換,從而完成對神經元形態的標注——就像我們身處于一個陌生的城市,根據手機地圖可以輕松定位到當前的位置——二維的標準腦圖譜就相當于手機地圖,我們結合自己看到的地標性建筑實現對手機地圖和所處實景的對應。
2015年,科學家們應用線臺掃描共聚焦(stage-scanning line confocal microscopy)進一步提高了成像速度。2016年,他們基于一種稱為全腦定位系統(Brain-wide Positioning System,BPS)的全自動顯微成像方法,通過在成像時同時染出細胞結構標志物,實現在單細胞分辨率水平的精準定位細胞結構。2021年,駱清銘團隊提出一種高清晰度、高通量的光學層析顯微成像新方法——線照明調制光學層析成像(Line illumination microscopy, LiMo),在快速高分辨率光學成像時能顯著提高背景抑制能力極大地提高了成像質量,提升了數據存儲與分析的效率。

fMOST成像過程展示
據報道,僅為攻克腦樣本制備的難題,駱清銘教授團隊耗費了三年時間。技術的研發涉及到生物、光學、機械、計算機數據處理等多學科領域的合作交叉。經過十幾年的研發與優化,fMOST技術具備高分辨率、高通量、高清晰度的優點,自動成像快速高效且準確地獲取神經元的形態信息,為后續重構、分析全腦范圍神經元形態打下堅實的基礎,已經成為研究解析全腦介觀神經元連接圖譜的一大利器,在全世界范圍內廣泛應用。
和人類社會相似類似,每個人都是一個獨立的個體,但又由于一些相似的特征而被分成各個群體。神經元也會擁有一系列的特征標簽,基因表達,神經元形態,投射信息和電生理特性等。為了更清晰地認知神經元世界的運作規則,更高分辨率的細胞分群信息在神經生物學內變得尤為重要。通過更高分辨率的手段獲得的分群信息幫助我們捕獲那些已知投射和功能的集團,更重要的是揭示出潛在的新細胞群體,更系統全面地揭示大腦的工作原理。fMOST及其配套的分析手段發展為我們提供了繪制大腦聯接網絡的可能性,與其他技術手段結合構建神經元類型標準框架,幫助揭示大腦功能。目前建立全腦神經元聯接圖譜庫是世界各國打造全球腦科學中心的重要基礎。現詳細為大家分享fMOST技術是如何助力于腦科學研究的。
fMOST與多技術協作構建單神經元級別的全腦聯接圖譜
fMOST的一個主要用處在于構建全腦聯接圖譜,從而與多技術協作揭示高分辨率的神經元分群,幫助我們更好地闡釋大腦發揮功能的單元。中國科學院腦科學與智能技術卓越創新中心嚴軍研究組、徐寧龍研究組與華中科技大學蘇州腦空間信息研究院、武漢光電國家研究中心龔輝團隊合作在Nature Neuroscience 期刊以封面文章的形式在線發表了題為Single-neuron projectome of mouse prefrontal cortex(小鼠前額葉單細胞投射譜)的研究論文,其中很好地展示了fMOST技術的這一應用。
前額葉皮層在決策、工作記憶、注意力等高級認知功能中扮演重要角色,其結構和功能的異常會導致多種腦疾病。其投射范圍很廣,幾乎覆蓋大部分腦區,包括皮層、紋狀體、丘腦、中腦和后腦等。這篇文章使用自主開發的Fast Neurite Tracer (FNT)光學成像大數據神經元追蹤及分析軟件,系統性地重構了小鼠前額葉皮層6357個單神經元全腦投射圖譜,建立了國際上最大的小鼠全腦介觀神經聯接圖譜數據庫(圖 A);揭示了小鼠前額葉皮層內64種神經元投射亞型的空間分布規律,發現不同群之間存在不同的投射特征(圖B);闡明了前額葉內部模塊化的連接網絡和等級結構(圖C)。在構建全腦聯接網絡的同時,研究人員也致力于與多技術協作建立一個能夠整合多種分子空間遺傳信息與多方面表型性質的標準化神經元分型框架。該文章整合了神經環路與轉錄組細胞類型的聯系。通過逆向示蹤和熒光原位雜交技術獲得神經元轉錄組亞型與投射亞型的對應關系(圖D)。以往的研究利用群體示蹤技術來研究前額葉皮層神經元的全腦投射模式,并不能很好地解析前額葉腦聯接網絡的工作模式和等級結構。通過fMOST 技術實現的單細胞水平成像幫助揭示了前額葉皮層內部連接和外部投射的規律,并提出了前額葉皮層可能的工作模型。
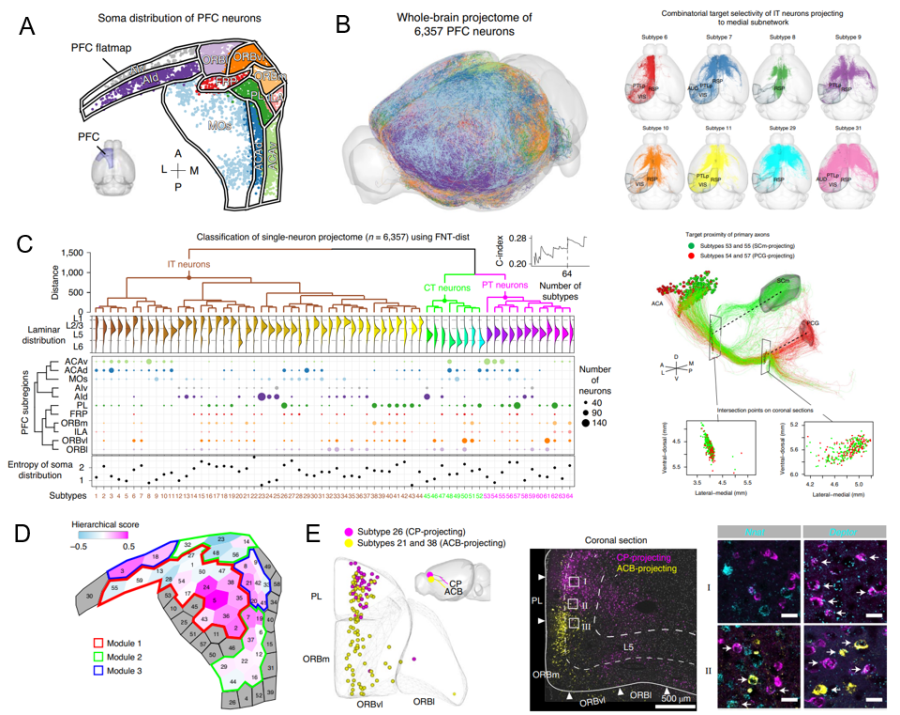
(A)重構mPFC神經元在腦內空間分布。(B)mPFC全腦軸突投射分布(右),幾種具有不同投射選擇性的神經元亞型(左)。(C)利用FNT 算法對單神經元投射圖譜進行聚類分析的結果(左),兩種差異性高亞型(SCm-projecting / PCG-projecting) 的三維重構結果(右)。(D前額葉內部連接網絡的模塊化和等級結構。(E)前額葉投射亞型與基因亞型的關系(CT皮層丘腦神經元在PL-ORB腦區)。
fMOST描繪精細神經元形態
單細胞水平的神經元精細結構解析能直觀的揭示神經元特性。fMOST可以在極高的分辨率下重構神經元形態,觀察神經元的精細結構。武漢光電國家研究中心駱清銘教授率領的MOST團隊與美國冷泉港實驗室黃佐實教授(Prof. Z. Josh Huang)課題組合作在Cell Reports發表的題了為Genetic Single Neuron Anatomy Reveals Fine Granularity of Cortical Axo-Axonic Cells(遺傳單神經元解剖學揭示皮層軸突-軸突細胞的精細結構)的文章,開發了fMOST在這一方面的具體應用。
在該文章中,研究者們設計了一種基于fMOST成像的,適用于遺傳特異標記的單細胞解剖學結構精準研究平臺(genetic Single Neuron Anatomy platform, gSNA)。通過解決單細胞遺傳標記、全腦精準成像、神經元重構和定量分析這四個方面的難點,實現了對AAC(Axo-Axonic Cells)細胞全腦單細胞尺度的解析。對全腦多個腦區的AAC細胞進行系統性的單神經元重建,發現AAC細胞的胞體位置、樹突和軸突纖維的空間分布模式不是隨機的,而是與大腦皮層分層相關。通過綜合大量重構細胞數據,利用合理定量手段及聚類分析對細胞分型,發現AAC細胞存在多種亞型。該研究全面的利用定量和定性手段解析了AAC細胞的形態學分型,更新了人們對AAC細胞的認知,有助于對AAC細胞的進一步理解和功能揭示。
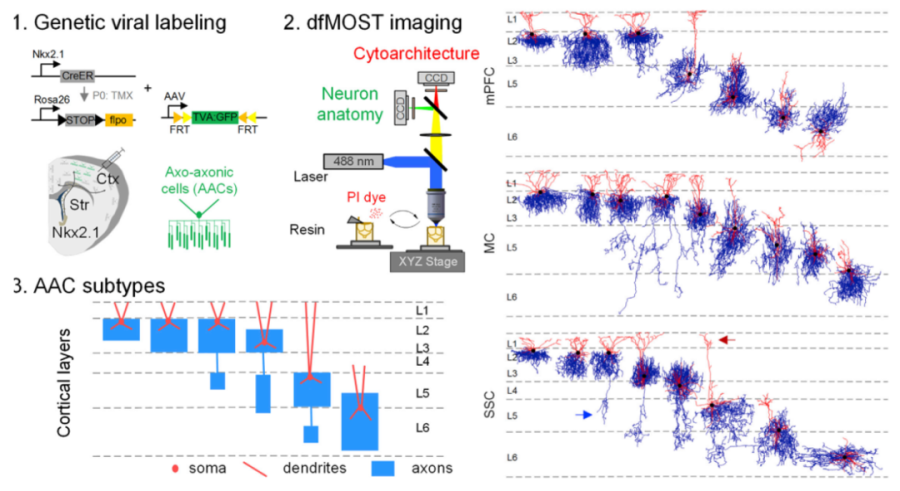
技術路線及皮層內AAC亞群分類結果
工欲善其事,必先利其器。生命科學的每一次發展,都以重大技術的進步為前提。fMOST技術為腦科學的發展做出了重大貢獻,極大推進了對大腦結構和功能的理解,從“看”得見,到“看”得清、“看”得懂。與現在使用的fMOST成像技術相比,電鏡可以很好地重構納米級分辨率的細胞微小結構,提供接近真實的細胞間聯接的狀態,完整的納米級/突觸分辨率的聯接圖譜提供了對環路有貢獻的所有信息。這些知識可用于揭示正常和病變狀態下環路特征并構建環路模型、識別功能相關的關鍵神經元,以及基于遠程連接和超微結構形態發現新的細胞類型。對秀麗隱桿線蟲和果蠅等模式生物的研究已經證明全腦聯接譜在支持神經環路深入研究方面的潛力。但是目前電鏡技術只能重構~1 mm3大小的結構,而小鼠大腦總體級約500 mm3,人的大腦則有小鼠的1000倍大。同時也對后續的數據分割、處理、存儲,運算等方面的技術水平要求大幅提高。但毫無疑問,獲得納米級的神經元聯接譜數據將在神經領域引起顛覆性的改變,也是后續腦圖譜繪制的發展目標之一。圖譜計劃的完善將奠定神經科學領域的基礎。覆蓋全腦范圍的聯接譜以及精確的胞間聯接結構繪制將徹底改變腦功能研究方式,從專注于假設驅動的研究到旨在闡明功能環路的基本規則的大型團隊協作項目。這些進展將為發現腦疾病相關的新環路機制奠定基礎,幫助解決腦疾病難題。
參考文獻:
1. Abbott L F, Bock D D, Callaway E M, et al. The mind of a mouse[J]. Cell, 2020, 182(6): 1372-1376.
2. Li A, Gong H, Zhang B, et al. Micro-optical sectioning tomography to obtain a high-resolution atlas of the mouse brain[J]. Science, 2010, 330(6009): 1404-1408.
3. Gong H, Zeng S, Yan C, et al. Continuously tracing brain-wide long-distance axonal projections in mice at a one-micron voxel resolution[J]. Neuroimage, 2013, 74: 87-98.
4. Yang T, Zheng T, Shang Z, et al. Rapid imaging of large tissues using high-resolution stage-scanning microscopy[J]. Biomedical optics express, 2015, 6(5): 1867-1875.
5. Gong H, Xu D, Yuan J, et al. High-throughput dual-colour precision imaging for brain-wide connectome with cytoarchitectonic landmarks at the cellular level[J]. Nature communications, 2016, 7(1): 1-12.
6. Zhong Q, Li A, Jin R, et al. High-definition imaging using line-illumination modulation microscopy[J]. Nature Methods, 2021, 18(3): 309-315.
7. Gao L, Liu S, Gou L, et al. Single-neuron projectome of mouse prefrontal cortex[J]. Nature Neuroscience, 2022: 1-15.
8. Wang X, Tucciarone J, Jiang S, et al. Genetic single neuron anatomy reveals fine granularity of cortical axo-axonic cells[J]. Cell reports, 2019, 26(11): 3145-3159.
作者:中國科學院腦科學與智能技術卓越創新中心 杜赟 王秋淼
 附件下載:
附件下載: